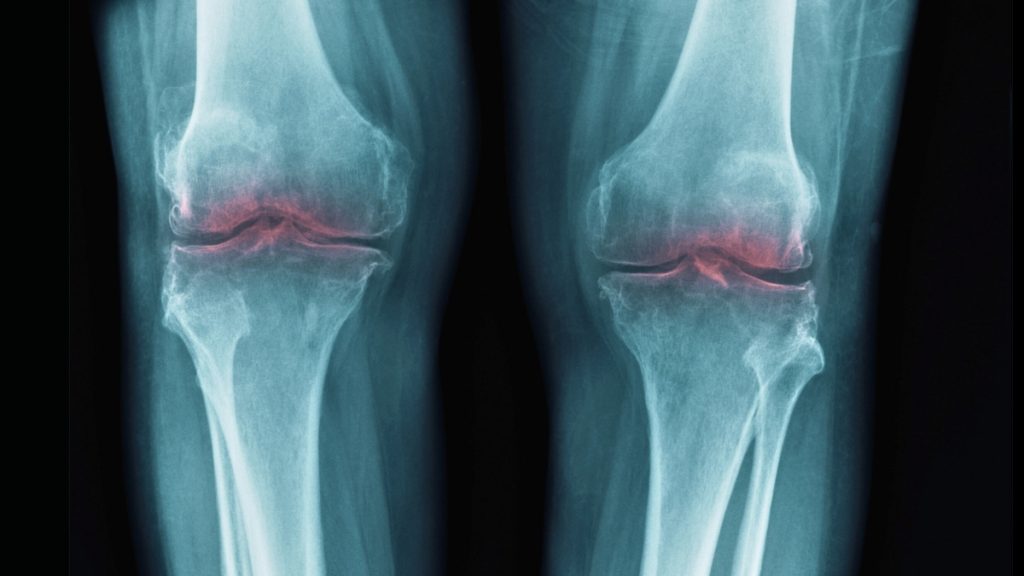
斯坦福大学的一项新研究在小鼠实验中发现,与年龄增长相关的软骨流失,可能主要由一种关键蛋白驱动。研究人员认为,这一发现为未来恢复老年人关节活动能力、缓解疼痛,甚至逆转骨关节炎带来了新的治疗方向。
这项研究将焦点锁定在一种名为 15-PGDH 的蛋白质上。科学界此前已经注意到,它在衰老过程中会逐渐增多,并抑制体内那些负责修复组织、降低炎症的有益分子。
研究团队因此提出一个关键问题:15-PGDH 是否正是骨关节炎发生的重要推手?
一种蛋白,可能触发软骨退化
在骨关节炎中,长期的关节受压会导致软骨中的胶原蛋白被破坏,继而引发炎症、僵硬和疼痛。如果15-PGDH在衰老过程中不断累积,那么它很可能会阻断软骨的自我修复能力。
为验证这一假设,研究人员在小鼠身上展开了一系列实验。
抑制15-PGDH,软骨出现“回春”
在实验中,研究人员为膝关节软骨已经磨损的小鼠注射了一种 15-PGDH 抑制剂。结果显示,原本变薄、退化的软骨开始重新增厚。
在另一组实验中,年轻但关节受伤的小鼠也接受了同样的处理。结果发现,这种抑制剂显著降低了损伤后常见的骨关节炎风险。
更引人注目的是,当研究人员人为制造出类似前十字韧带撕裂的损伤时,接受治疗的小鼠几乎没有发展出骨关节炎——而在传统的小鼠模型中,这种结果通常难以避免。
不靠干细胞,身体自己修复
过去,软骨再生的研究往往寄希望于干细胞。但在这项研究中,干细胞并不是主角。
当15-PGDH被抑制后,原本负责生成和维持软骨的软骨细胞本身发生了变化,它们转变为更健康、更具修复能力的状态,从而推动组织再生。
微生物学家海伦·布劳(Helen Blau)表示,这代表了一种全新的成人组织再生机制。
她指出,这一策略在治疗因衰老或损伤引起的关节炎方面,具有显著的临床潜力。
“我们一直在寻找干细胞的作用,但现在看来,它们并没有参与其中,”她说,“这让人非常兴奋。”
行为改善,疼痛明显减轻
组织层面的变化也反映在小鼠的行为上。
接受治疗的小鼠行走更加稳定,受伤腿部的承重能力提高,这些变化通常被视为疼痛减轻和功能改善的信号。
研究人员的影像分析显示,经过处理的老化软骨在结构和密度上,更接近年轻健康的软骨状态。
人体组织实验,结果同样积极
除了动物实验,研究团队还在接受膝关节置换手术患者的人体软骨样本上进行了测试。
结果同样令人振奋:软骨组织表现出更强的硬度,炎症相关标志明显减少,并出现再生迹象。
骨科医生 Nidhi Bhutani 表示,这一发现正在改变人们对组织再生机制的理解。
她指出,软骨中原本就存在的大量细胞,能够通过改变基因表达模式,重新承担修复功能。
“如果我们能够针对这些现有细胞进行再生治疗,临床上的整体影响可能会非常大,”她说。
未来或不再依赖关节置换?
尽管研究仍处于早期阶段,但科学家认为,这一机制最终有望带来真正针对病因的骨关节炎治疗方法,而不仅仅是缓解症状。
目前,骨关节炎的临床治疗手段仍主要集中在止痛和功能管理上,髋关节或膝关节置换往往是终极选择。尽管近年研究不断推进,但尚无成熟方案能够逆转软骨退化本身。
临床试验或将加速推进
研究团队表示,下一步很可能是开展人体临床试验。
此前,一种用于治疗肌肉衰弱的 15-PGDH 抑制剂 已完成安全性测试,并未发现明显风险,这为类似药物在骨关节炎领域的应用铺平了道路。
布劳表示,团队对这一潜在突破充满期待。
“如果我们能够重新生长原有的软骨,就有可能避免关节置换手术,”她说。
这项研究或许标志着一个新的方向:让身体自己修复,而不是被动替换。
来源:sciencealert(编译 / 整理:olaola)
